Evrendeki tüm madde ve cisimlerin en küçük yapı taşıdır. Bölünemez anlamına gelen atomus kelimesinden türetilmiştir. İlk olarak Milattan Önce 440’lı yıllarda yaşamış olan Demokritos tarafından ortaya atılmıştır. Tarihçesine bakıldığı zaman ünlü filozof Aristoteles’in de çeşitli çalışmalar yürüttüğü görülmüştür.
Aristo’ya göre madde; ateş, su, toprak ve hava olmak üzere 4 ana bileşenden oluşmaktadır. 1803 yılında John Dalton ise modern atom teorisini geliştirmiştir. Dalton, kimyasal reaksiyonlarda maddenin tam sayılarla belirlenen oranlarda tepkimeye girdiğini bulmuştur.
[renkbox baslik=”Kimyasal Bağlar Nedir? Çeşitleri Nelerdir?” link=”https://bilgihanem.com/kimyasal-baglar-nedir/” resim=”https://bilgihanem.com/wp-content/uploads/2016/02/kimyasal-baglar-nedir-cesitleri-nelerdir.png” renk=”mavi” yenisekme=”evet”][/renkbox]Atomun hem kendi içerisinde hem de diğer atomlarla olan hareketlerini düzenlemek için 4 ana kuvvet bulunmaktadır. Bunlar; zayıf, çekim, elektromanyetik ve nükleer kuvvetlerdir. Örneğin; gezegenleri Güneş Sistemi’nde tutan çekim kuvvetidir. Aynı zamanda atom ve molekülleri bir arada tutan da bu kuvvettir.
Atom Nedir?
 Madde denilen varlığın en küçük parçası olan ve aynı zamanda temel yapı taşına atom adı verilir. Madde boşlukta yer tutan ve bir ağırlığı olan herhangi bir varlığa denir. Tüm maddeleri oluşturan 105 adet farklı element olduğu bilinmektedir.
Madde denilen varlığın en küçük parçası olan ve aynı zamanda temel yapı taşına atom adı verilir. Madde boşlukta yer tutan ve bir ağırlığı olan herhangi bir varlığa denir. Tüm maddeleri oluşturan 105 adet farklı element olduğu bilinmektedir.
Bilinen bu elementlerin her birini oluşturan en küçük yapı taşlarına atom diyoruz. Örneğin; bir hidrojen ve bir demir birer elementtir. Çünkü bu iki elementte de çeşitli atomlar vardır. Çeşitli atomların bir araya gelmesindense bileşik denen maddeler oluşur.
Örneğin; su bir element değildir, bileşiktir. Su, ateş, toprak gibi çevremizde sıkça gördüğümüz maddelerin hepsi atomların bir araya gelmesi ile oluşmuştur.
Atomun Yapısal Özellikleri Nelerdir?
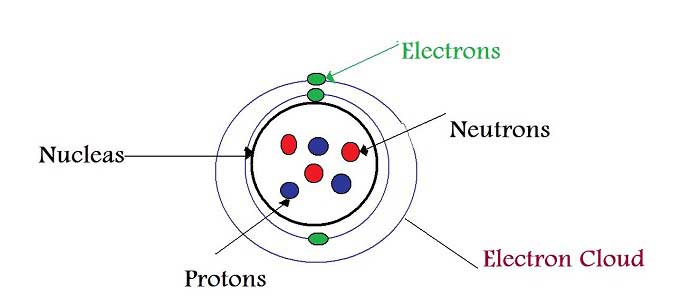 Bir atomun temel yapısında iki ana bölge bulunmaktadır. Bunlar; çekirdek ve enerji katmanlarıdır. Atom çekirdeği, proton ile nötronların bulunduğu, yoğun ve küçük hacimli olan bölgedir. Pozitif yüklü tanecikler olan protonlar, atomun cinsini belirlemektedir. Nötr atomlarda ise elektron sayıları eşittir. Protonlar, atomun kütlesine etki etmektedir.
Bir atomun temel yapısında iki ana bölge bulunmaktadır. Bunlar; çekirdek ve enerji katmanlarıdır. Atom çekirdeği, proton ile nötronların bulunduğu, yoğun ve küçük hacimli olan bölgedir. Pozitif yüklü tanecikler olan protonlar, atomun cinsini belirlemektedir. Nötr atomlarda ise elektron sayıları eşittir. Protonlar, atomun kütlesine etki etmektedir.
Yüksüz olan nötronlar ise atomun kimyasal özelliklerine etki etmezler. Yalnızca kütlesine etki ederler. Negatif yüklü elektronlar, atom çekirdeğinin etrafında hareket ederler ve atomun yüküne etkileri vardır. Özellikle değerlik elektronları, atomun kimyasal özelliklerine etki etmektedir. Ama atomun kütlesine etkileri ihmal edilmektedir.
Enerji katmanları ise elektronların dağıldığı, çekirdek hacmine göre oldukça büyük ve boşlukların çok olduğu bölgedir. Çekirdekte pozitif yüklü protonlar ve yüksüz nötronlar vardır. Enerji katmanlarında ise sadece negatif yüklü elektronlar bulunur. Bu yüklere göre atomlar farklı isimler almaktadır. Bunlara bakacak olursak;
İzotop Atom: Proton sayıları aynı, nötron sayıları ise farklı olan türdür. Bu atomların nötron sayıları farklı olduğu için kütle numaraları da farklıdır.
İzoton Atom: Proton sayıları farklı, nötron sayıları aynı olan türdür. Hem kimyasal hem de fiziksel özellikleri farklıdır.
İzobar Atom: Proton sayıları farklı, kütle numaraları yani nükleon sayıları aynı olan elementlerdir. Hem kimyasal hem de fiziksel özellikleri farklıdır.
Allotrop Atom: Bir elementin özdeş atomlarının farklı sayı ve dizilişteki şekillerini ifade etmektedir. Bunlar aynı elementlere ait olduğu için kimyasal özellikleri de aynıdır. Atomlar, farklı sayı ve dizilişte olduğu için fiziksel özellikleri de farklıdır.
Atomların en temel yapısal özellikleri şunlardır:
- Atom, bölünemez ve parçalanamaz.
- Çıplak gözle ya da en gelişmiş elektron mikroskobu ile görülemez.
- Küre şeklinde olan atomlar, boşluklu ve elektrikli bir yapıya sahiptirler. Elektrikli yapıya sahip olması, içindeki artı (+) ve eksi (-) yüklü taneciklerden kaynaklanmaktadır.
- Çekirdeğinin parçalanmasıyla atom bombaları yapılmaktadır ve nükleer enerji santrallerinde enerji üretilmektedir.
- Maddenin sahip olduğu bütün özellikleri taşımaktadır.
- Atomlar birbirleriyle etkileşip bir araya tutunurlar ve maddeyi oluştururlar. Maddeyi oluşturan en küçük birim taneciklerdir. Bunlar ise atom veya molekülleri temsil etmektedir.
- Atom veya moleküllerin maddeyi oluşturabilmesi için bir arada bulunması için birbirine çekim kuvveti uygularlar.
- Maddeyi oluşturan moleküller arasındaki çekim kuvveti zayıf iken, molekülleri oluşturan atomlar arasındaki çekim kuvvetti güçlüdür.
- Aynı molekülü oluşturan atomlar birbirine daha yakın iken, farklı molekülleri oluşturan atomlar birbirine uzaktır.
- Atomik yapılı elementleri oluşturan ve birbiri ile temas halinde olan atomlara, bağlı atom denmektedir.
Günümüzde kabul edilen ve geçerliliği süren son atom teorisi, Kuantum Atom Teorisi’dir. Kuantum Atom Teorisi’ne göre atomun merkezinde bulunan çekirdeğin etrafındaki elektronlar belli bölgelerde bulunurlar. Bu bölgelere orbital denir.
Belli enerji seviyesine sahip orbitaller atomu oluşturan küresel katmanlarda yer almaktadır. Portakal kabuğu şeklinde iç içe geçmiş bu orbitallerin, belli şekilleri ve açıları bulunmaktadır.
Bir atomun çapı 10-8 cm civarındadır. Atomun çekirdeğinin çapı 10-13 cm’dir. Atomların yapısını incelemek, pozisyonlarını gözlemlemek için elektron mikroskobu, x ışını mikroskobu ve nükleer manyetik rezonans spektroskopisi kullanılmaktadır.
Atom Modelleri Nelerdir?
 Bilinmesi gereken önemli atom modelleri ve yaratıcılarının ortaya koyduğu kuramları hakkında bilgiler şu şekildedir:
Bilinmesi gereken önemli atom modelleri ve yaratıcılarının ortaya koyduğu kuramları hakkında bilgiler şu şekildedir:
Dalton Atom Modeli
Günümüzdeki atom modelinin temellerinin atıldığı atom modelidir. Bu modelin temelini 1805 yılında John Dalton atmıştır. Bu kurama göre elementler, kimyasal açıdan birbiriyle aynı olan atom parçaları içerir.
Dalton, kimyasal tepkimelere giren çeşitli maddelerin arasındaki kütlesel ilişkilere dayanarak, atomların bağıl kütle değerlerini de bulmuştur. Günümüz modern atom kuramı, Dalton’un atom kuramına uzanır ama haliyle günümüzde bazı değişikliklere uğramıştır.
Dalton’un keşfetmiş olduğu atom modeli, maddeyi anlayabilmek, atomun özelliklerini ortaya çıkması bakımından çok yarar sağlamıştır. Sonraki araştırmaların temelini oluşturduğundan bilimsel anlamda ilk atom teorisi kabul edilmiştir. Dalton kuramı üç kurala dayanır. Bunlar;
- Tek başına bir elementin içinde bulunan tüm atomların kütle değeri ve özellikleri aynı olmakla beraber; farklı diğer elementlerin atomlarından ayrılır.
- Bilinen elementler, atom olarak isimlendirilmiş bölünme özelliği olmayan minik tanelerden meydana gelmiştir. Atom denen varlıklar, kimyasal tepkimelere katılmazlar ve bölünemezler.
- Kimyevi bir bileşik iki ve daha fazla elementin bir oranda birliktelik göstermesi ile meydana gelirler.
Thomson Atom Modeli
Thomson elektron olarak bilinen olgunun keşfini yapmıştır. Thomson; elektronu farklı gazlarla, çeşitli deneyler yaparak; atomların elektron yükü/kütlesi biçimindeki oranı hesaplayarak keşfetmiştir. Thomson’a göre elektron veren atom (+) yüklüdür ve bunu da ispatlamıştır.
Thomson atom modeline, üzümlü kek modeli adı da verilmektedir. Bunun sebebi; atom içindeki elektron ve protonun homojen formda dağılmasıdır. Sonraları ortaya çıkan Rutherford modeli ile bu homojen dağılım kuramının yanlış olduğu ispatlanmıştır.
Bu yeni ilkeye göre; yine atom artı yüklüdür ama içindeki elektronlar madde içinde gömülü biçimdedir ve hareket etme özelliğine sahip değillerdir. İçerideki bu elektronların kütleleri oldukça küçük olduğundan atomun kütle ağırlığını artı yüklü olan madde meydana getirir. Bu ilkede atom küre şeklinde belirtilmiştir.
Rutherford Atom Modeli
Atomla ilgili çalışmaların temelinde çok önemli bir yere sahip olan bir diğer atom modeli Rutherford’dur. Modele göre atom küre biçimindedir. Merak konusu olan durum; proton ve elektronun atom parçacığı içinde nasıl yerleştiğidir.
Rutherford araştırmasını yaparken bu sorunun cevabını aramıştır ve neticesinde alfa parçacıkları adlı deneyi yaptıktan sonra bir model ortaya çıkartmıştır. Sonuçta atom içindeki pozitif yük taşıyan ve kütlesi büyükçe olan parçanın hacminin, atomun toplam hacmine göre daha küçük olması gerektiği kanısına varmış ve bu parçaya çekirdek ismini vermiştir.
[renkbox baslik=”Asit – Baz Kavramları: Asit ve Bazlar Nedir? Genel Özellikleri Nelerdir?” link=”https://bilgihanem.com/asit-baz-nedir/” resim=”https://bilgihanem.com/wp-content/uploads/2015/01/asit-ve-baz-nedir-genel-ozellikleri.png” renk=”kirmizi” yenisekme=”hayir”][/renkbox]Çekirdek ve atom arasındaki boyut ilişkisi, Rutherford’un açıklamasına göre şu şekilde açıklanabilir: Bir çekirdek tenis topu kadar büyük olsaydı, atom denen olgu stadyum kadar büyük olurdu.
Bohr Atom Modeli
Kendisinden önceki tüm atom modellerinin bilgilerinden faydalanarak yeni bir atom modeli oluşturan Bohr, bu buluşu 1919 yılında yapmıştır. Bohr’a kadar yapılan çalışmalarda elektronların varlığı ve özellikleri belirlenmişti ancak elektronların yörüngeleri, hızları gibi durumlarla ilgili bilgiler yetersizdi.
Bohr, atom incelemesini genel olarak bu yönde yapmıştır. Atom parçasının içindeki elektronlar, merkezde bulunan çekirdekten belirli bir uzaklıkta bulunur ve bu mesafeyi bozmadan hareket eder.
Elektronların hareket etme ihtimalinin olduğu seviyeler; K, L, M, N, O harfleri ile sembolize edilir. Günümüzdeki bilgilere göre ise Bohr kuramında geçerli olan elektronların daire biçiminde bir yörünge çizdikleri ilkesi yanlıştır.








 Aykut SARITAŞ Bilgi Paylaşım Sitesi !
Aykut SARITAŞ Bilgi Paylaşım Sitesi !